12二溴乙烷可作汽油_12二溴乙烷转化为乙二醇
1.求年上海高考化学试卷和答案
2.当乙烯与含氯化钠的溴的水溶液反应,产物为什么没有1,2二溴乙烷
3.Ⅰ.下图是某学生绘制的实验室蒸馏石油的装置图:(1)实验室分馏石油的正确操作顺序是______A.连接接液
4.十万火急!!!!关于化学!!拜托了!!! 悬赏分:200
二溴乙烷化学式:C?H?Br?。
二溴乙烷,是一种有机化合物,主要用作溶剂,也可用于有机合成。2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,二溴乙烷在2A类致癌物清单中。
狭义上的有机化合物主要是指由碳元素、氢元素组成,一定是含碳的化合物,但是不包括碳的氧化物和硫化物、碳酸、碳酸盐、氰化物、硫氰化物、氰酸盐、碳化物、碳硼烷、羰基金属、不含M-C键的金属有机配体配合物,部分金属有机化合物等主要在无机化学中研究的含碳物质。
有机物是生命产生的物质基础,所有的生命体都含有机化合物,如脂肪、氨基酸、蛋白质、糖、血红素、叶绿素、酶、激素等。生物体内的新陈代谢和生物的遗传现象,都涉及到有机化合物的转变。
此外,许多与人类生活有密切相关的物质,如石油、天然气、棉花、染料、化纤、塑料、有机玻璃、天然和合成药物等,均与有机化合物有着密切联系。
有机物的主要特点是:
1、大多为共价型化合物,固态是分子晶体,有较低的熔点(一般在300℃以下) 、沸点,极性较小,属于非电解质。
2、大多易燃,受热易分解。
3、多数难溶于水,易溶于乙醇、、丙酮、苯、汽油等有机溶剂。
4、有机物的反应多为分子反应,反应速度较慢,常需要加热、光照或催化剂。
5、有机反应的副反应多,产率较低,产物往往是混合物。
6、普遍存在同分异构现象。
求年上海高考化学试卷和答案
四氟二溴乙烷
别名 氟里昂一114B一2
英文名 Sym-Dibrometetrafluoroethane; Freon
114B—2
分子式 CF2Br-CF2Br
分子量 259.82
性状 液体,低毒,密度2.18克/厘米2(21.1℃),沸
点47.3℃,熔点-112℃。不燃。
来源 四氟乙烯与溴两次加成,经冷凝、中和、精馏、
分离、得产品。
包装 用铁桶包装,每桶净重200公斤。
用途 可作高效灭火剂,还可作冷却剂,高温气体润
滑剂,亦可用于传热介质等。
储运条件 储存于阴凉通风处、避光、避热。
当乙烯与含氯化钠的溴的水溶液反应,产物为什么没有1,2二溴乙烷
年上海用的是全国卷吧?我有.你要要的话给我发邮件.或到我的空间下载.我给你传上去.
19年全国普通高等学校招生考试
化学试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷1至4页,第Ⅱ卷5至10页,共150分.考试时间120分钟.
第Ⅰ卷 (选择题 共84分)
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、准考证号、考试科目用铅笔涂写在答题卡上.
2.每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案,不能答在试题卷上.
3.考试结束,监考人将本试卷和答题卡一并收回.
可能用到的原子量:
H 1 C 12 N 14 O 16 F 19 S 32
CI 35.5 Fe 56 Cu 64 Br 80 I 127
一.选择题(本题包括5小题,每小题3分,共15分.每小题只有一个选项符合题意.)
1.19世纪中叶,门捷列夫的突出贡献是
(A)提出原子学说 (B)发现元素周期律
(C)提出分子学说 (D)发现氧气
2.下列各组微粒中,核外电子总数相等的是
(A)K+和Na+ (B)CO2和NO2
(C)CO和CO2 (D)N2和CO
3.将某溶液逐滴加入Fe(OH)3溶胶内,开始时产生沉淀,继续滴加时沉淀又溶解,该溶液是
(A)2 mol?L-1H2SO4溶液 (B)2 mol?L-1NaOH溶液
(C)2 mol?L-1MgSO4溶液 (D)硅酸溶胶
4.已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(-OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是
5.钢铁发生吸氧腐蚀时,正极上发生的电极反应是
(A)2H++2e- =H2 (B)Fe2++2e- =Fe
(C)2H2O+O2+4e-=4OH- (D)Fe3++e-=Fe2+
二.选择题(本题包括15小题,每小题3分,共45分.每小题有一个或两个选项符合题意.若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分,但只要选错一个,该小题就为0分.)
6.甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是:
(CH3)2C=O+HCN—→(CH3)2C(OH)CN
(CH3)2C(OH)CN+CH3OH+H2SO4—→CH2=C(CH3)COOCH3+NH4HSO4
90年代新法的反应是:CH3C≡CH+CO+CH3OH CH2=C(CH3)COOCH3
与旧法比较,新法的优点是
(A)原料无爆炸危险 (B)原料都是无毒物质
(C)没有副产物,原料利用率高 (D)对设备腐蚀性较小
7.下列叙述中,正确的是
(A)含金属元素的离子不一定都是阳离子
(B)在氧化还原反应中,非金属单质一定是氧化剂
(C)某元素从化合态变为游离态时,该元素一定被还原
(D)金属阳离子被还原不一定得到金属单质
8.某溶液含有较多的Na2SO4和少量的Fe2(SO4)3.若用该溶液制取芒硝,可供选择的操作有:
①加适量H2SO4溶液,②加金属Na,③结晶,④加过量NaOH溶液,
⑤加强热脱结晶水,⑥过滤.正确的操作步骤是
(A)②⑥③ (B)④⑥①③ (C)④⑥③⑤ (D)②⑥①③⑤
9.下列各组离子,在强碱性溶液中可以大量共存的是
(A) I- AlO2- Cl- S2-
(B) Na+ K+ NH4+ Ba2+
(C) Br- S2- Cl- CO32-
(D) SO32- NO3- SO42- HCO3-
10.已知铍(Be)的原子序数为4.下列对铍及其化合物的叙述中,正确的是
(A)铍的原子半径大于硼的原子半径
(B)氯化铍分子中铍原子的最外层电子数是8
(C)氢氧化铍的碱性比氢氧化钙的弱
(D)单质铍跟冷水反应产生氢气
11.分别取等质量80℃的甲、乙两种化合物的饱和溶液,降温至20℃后,所析出的甲的质量比乙的大(甲和乙均无结晶水).下列关于甲、乙溶解度的叙述中肯定正确的是
(A)20℃时,乙的溶解度比甲的大 (B)80℃时,甲的溶解度比乙的大
(C)温度对乙的溶解度影响较大 (D)温度对甲的溶解度影响较大
12.下列反应的离子方程式正确的是
(A)氨气通入醋酸溶液中 CH3COOH+NH3=CH3COONH4
(B)澄清的石灰水跟盐酸反应 H++OH-=H2O
(C)碳酸钡溶于醋酸 BaCO3+2H+=Ba2++H2O+CO2↑
(D)金属钠跟水反应 2Na+2H2O=2Na++2OH-+H2↑
13.向50mL 18 mol?L-1H2SO4溶液中加入足量的铜片并加热.充分反应后,被还原的H2SO4的物质的量
(A)小于0.45 mol (B)等于0.45 mol
(C)在0.45 mol和0.90 mol之间 (D)大于0.90 mol
14.0.1 mol?L-1NaOH和0.1 mol?L-1NH4Cl溶液等体积混合后,离子浓度大小正确的次序是
(A)[Na+]>[Cl-]>[OH-]>[H+] (B)[Na+]=[Cl-]>[OH-]>[H+]
(C)[Na+]=[Cl-]>[H+]>[OH-] (D)[Cl-]>[Na+]>[OH-]>[H+]
15.下列说法正确的是(N0表示阿伏加德罗常数的值)
(A)在常温常压下,11.2 L N2含有的分子数为0.5N0
(B)在常温常压下,1 mol Ne含有的原子数为N0
(C)71 g Cl2所含原子数为2N0
(D)在同温同压时,相同体积的任何气体单质所含的原子数相同
16.CaC2和MgC2都是离子化合物.下列叙述中正确的是
(A) MgC2和CaC2都能跟水反应生成乙炔
(B) C22-的电子式为
(C) CaC2在水中以Ca2+和C22-形式存在
(D) MgC2的熔点低,可能在100℃以下
17.将0.1 mol下列物质置于1 L水中充分搅拌后,溶液中阴离子数最多的是
(A)KCl (B)Mg(OH)2 (C)Na2CO3 (D)MgSO4
18.在室温下等体积的酸和碱的溶液,混合后pH值一定小于7的是
(A)pH=3的硝酸跟pH=11的氢氧化钾溶液
(B)pH=3的盐酸跟pH=11的氨水
(C)pH=3的硫酸跟pH=11的氢氧化钠溶液
(D)pH=3的醋酸跟pH=11的氢氧化钡溶液
19.反应2X(气)+Y(气) 2Z(气)+热量,在不同温度(T1和T2)及压强(P1和 P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是
(A)T1<T2,P1<P2 (B)T1<T2,P1>P2
(C)T1>T2,P1>P2 (D)T1>T2,P1<P2
20.两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L.下列各组混合烃中不符合此条件的是
(A)CH4 C2H4 (B)CH4 C3H6 (C)C2H4 C3H4 (D)C2H2 C3H6
三.选择题(本题包括6小题,每小题4分,共24分.每小题只有一个项符合题意.)
21. 为实现中国2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在.已知在溶液中IO3-可和I-发生反应:
IO3-+5I-+6H+=3I2+3H2O根据此反应,可用试纸和一些生活中常见的物质进行实验,证明在食盐中存在IO3-.可供选用的物质有:①自来水,②蓝色石蕊试纸,③碘化钾淀粉试纸,④淀粉,⑤食糖,⑥食醋,⑦白酒.进行上述实验时必须使用的物质是
(A)①③ (B)③⑥ (C)②④⑥ (D)①②④⑤⑦
22.密度为0.91 g.cm-3的氨水,质量百分比浓度为25%(即质量分数为0.25),该氨水用等体积的水稀释后,所得溶液的质量百分比浓度
(A)等于12.5% (B)大于12.5% (C)小于12.5% (D)无法确定
23.若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为
(A)10(a+b-12)% (B)10(a+b-14)% (C)10(12-a-b)% (D)10(14-a-b)%
24.某金属单质跟一定浓度的硝酸反应,定只产生单一的还原产物.当参加反应的单质与被还原硝酸的物质的量之比为2:1时,还原产物是
(A)NO2 (B)NO (C)N2O (D)N2
25.X、Y、Z和R分别代表四种元素.如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的原子序数),则下列关系正确的是
(A)a-c=m-n (B)a-b=n-m (C)c-d=m+n (D)b-d=n+m
26.一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量是
(A)1.4 g (B)2.2 g (C)4.4 g (D)在2.2 g和4.4 g之间
第Ⅱ卷 (非选择题 共66分)
注意事项:1.第Ⅱ卷共6页,用钢笔或圆珠笔直接答在试题卷上.
2.答卷前将密封线内的项目填写清楚.
四.(本题包括2小题,共14分)
27.(4分)进行化学实验必须注意安全,下列说法正确的是(填写标号)_______.
(A)不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
(B)不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
(C)如果苯酚浓溶液沾到皮肤上,应立即用酒精洗
(D)配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
28.(10分)1,2 — 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g?cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2- 二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
___________________________________________________________
___________________________________________________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请
写出发生堵塞时瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因.___________________________________________________________
_______________________________________________________________
五.(本题包括3小题,共17分)
29.(5分)(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:____________________________________________.
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:________________________________________________________.
30.(5分)试样X由氧化亚铁和氧化铜组成.取质量相等的两份试样按下图所示进行实验:
(1)请写出步骤③中所发生的全部反应的离子方程式.
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为_____________.(用m表示)
31.(7分)某无色溶液可能含有下列钠盐中的几种:(A)氯化钠 (B)硫化钠
(C)亚硫酸钠 (D)硫代硫酸钠 (E)硫酸钠 (F)碳酸钠.向此溶液中加入适量稀硫酸,有浅**的沉淀析出,同时有气体产生.此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色.根据上述实验现象回答下列问题.
(1)不能使品红试液褪色,说明该气体中不含____________(填分子式).
(2)此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母).
第一种情况是____________,第二种情况是____________,
第三种情况是____________,第四种情况是____________.
(可不填满,也可补充)
六.(本题包括3小题,共17分)
32.(4分)有机化学中取代反应范畴很广.下列6个反应中,属于取代反应范畴的是(填写相应的字母)_______________________.
33.(6分)通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
下面是9个化合物的转变关系
(1)化合物①是__________________,它跟氯气发生反应的条件A是__________________.
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨,⑨的结构简式是__________________,名称是__________________.
(3)化合物⑨是重要的定香剂,香料工业上常用化合物②和⑧直接合成它.此反应的化学方程式是_________________________________________________.
34.(7分)A、B都是芳香族化合物,1 mol A水解得到1 mol B和1 mol醋酸.A、B的分子量都不超过200,完全燃烧都只生成CO2和H2O.且B分子中碳和氢元素总的质量百分含量为65.2%(即质量分数为0.652).A溶液具有酸性,不能使FeCl3溶液显色.
(1)A、B分子量之差为_______________.
(2)1个B分子中应该有_______________个氧原子.
(3)A的分子式是_______________.
(4)B可能的三种结构简式是:
_______________、_______________、_______________.
七.(本题包括2小题,共18分)
35.(6分)将8.8 g FeS固体置于200 mL 2.0 mol?L-1的盐酸中,以制备H2S气体.反应完全后,若溶液中H2S的浓度为0.10 mol?L-1,定溶液体积不变,试计算:
(1)收集到的H2S气体的体积(标准状况).
(2)溶液中Fe2+和H+的物质的量浓度(摩尔浓度).
36.(12分)1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为30.
请回答下列问题:
(1)固体C60与金刚石相比较,熔点较高者应是____________,理由是:
_________________________________________________________.
(2)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)_________,并简述其理由:___________________________________.
(3)通过计算,确定C60分子所含单键数.
C60分子所含单键数为_______________.
(4)C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知.通过计算确定C70分子中五边形和六边形的数目.
C70分子中所含五边形数为____________,六边形数为_________.
19化学试题答案及评分标准
说明:
1.本答案供阅卷评分使用,考生若写出其它正确答案,可参照评分标准给分.
2.化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分.
3.化学方程式、离子方程式未配平的,都不给分.
一.(本题包括5小题,每小题3分,共15分)
1.B 2.D 3.A 4.C 5.C
二.(本题包括15小题,每小题3分,共45分)
6.C、D 7.A、D 8.B 9.A、C 10.A、C
11.D 12.B、D 13.A 14.B 15.B、C
16.A、B 17.C 18.D 19.C 20.B、D
三.(本题包括6小题,每小题4分,共24分)
21.B 22.C 23.A 24.C 25.D 26.A
四.(本题包括2小题,共14分)
27.(4分)
A、B、C (对1个1分,对2个3分,全对4分,错1个扣1分)
28.(10分)
(1)
CH2=CH2+Br2→CH2BrCH2Br (每式1分,共2分)
(2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出. (2分)
(3)除去乙烯中带出的酸性气体.或答除去CO2、SO2. (2分)
(4)原因:
①乙烯发生(或通过液溴)速度过快
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答"控温不当"亦可)
(两点各2分,共4分.答其它原因不给分也不扣分)
五.(本题包括3小题,共17分)
30.(5分)
(1) Cu2++Fe====Cu+Fe2+ 2H++Fe=Fe2++H2↑(每式1分,共2分)
31.(7分)
(1) SO2 (2分)
(2) B、C、F B、D、F
(对1空给2分,对两空给5分.每错1空,倒扣3分,不出现负分)
六.(本题包括3小题,共17分)
32.(4分)A、C、E、F (4分)
(每对一个给1分,每错1个倒扣2分,不出现负分)
33.(6分)
34.(7分)
(1)42 (1分) (2)3 (2分) (3)C9H8O4 (1分)
过200-42=158.A有羧基,所以,B也有羧基,且有从A(醋酸酯)水解释出的羟基,初步推测可能含3个氧原子.从B分子中氧的百分含量(由题意推出),可求B的分子量
由数据可以确认,B分子为羟基苯甲酸.
七.(本题包括2小题,共18分)
35.(6分)根据方程式FeS+2H+====Fe2++H2S↑可判断盐酸过量,计算应以FeS的物质的量为基准.
(1)共生成H2S 0.10mol.在溶液中溶解的物质的量为:
0.10 mol?L-1×0.20 L=0.020 mol
所以收集到H2S气体的物质的量为:0.10 mol-0.020 mol=0.08 mol
收集到H2S气体的体积(标准状况)为:
22.4 L?mol-1×0.08 mol=1.8 L (2分)
消耗掉H+0.20 mol,反应前H+的物质的量为:
2.0 mol?L-1×0.20 L=0.40 mol
36.(12分)
(1) 金刚石
金刚石属原子晶体,而固体C60不是,故金刚石熔点较高. (1分)
(答出“金刚石属原子晶体”即给分)
(2) 可能
因C60分子含30个双键,与极活泼的F2发生加成反应即可生成C60F60 (1分)
(只要指出"C60含30个双键"即给分,但答“因C60含有双键”不给分)
也可由欧拉定理计算键数(即棱边数):60+(12+20)-2=90
C60分子中单键为:90-30=60 (1分)
(答“2×30(双键数)=60”即给2分)
(4)设C70分子中五边形数为x,六边形数为y.依题意可得方程组:
解得:五边形数x=12,六边形数y=25 (各1分)
Ⅰ.下图是某学生绘制的实验室蒸馏石油的装置图:(1)实验室分馏石油的正确操作顺序是______A.连接接液
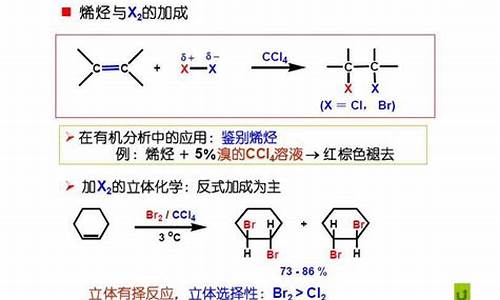
是因为乙烯与溴的反应不是一步完成的。
当溴分子接近双键时,由于π电子的排斥,使非极性的溴溴键发生极化,离π键近的溴原子带部分正电荷,另一溴原子带部分负电荷。带部分正电荷的溴原子对双键的亲电进攻,生成一个环状的溴鎓正离子。 然后么,溴或者氯阴离子进攻溴鎓离子,得到1,2-二溴乙烷。
1,2-二溴乙烷,无色液体,有挥发性,有毒。微溶于水,溶于乙醇、、氯仿、丙酮等有机溶剂。性质稳定,常与四乙基铅同时加在汽油中,可使燃烧后产生的氧化铅变为具有挥发性的溴化铅,从内燃机中排出。用作脂肪、油、树脂等的溶剂,谷物和水果等的杀菌剂、木材的杀虫剂等。可由乙烯与溴加成制得。
十万火急!!!!关于化学!!拜托了!!! 悬赏分:200
Ⅰ.(1)按组装仪器的顺序从下到上,从左到右,连接好装置后,注意先检验装置气密性,再装入碎瓷片和石油进行蒸馏,正确操作顺序为:EFDACBG,
故答案为:EFDACBG;
(2)①温度计水银球应处于蒸馏烧瓶支管口处,不应插入溶液;
②冷凝管中凝水的流向错误,冷水应从下口进,上口出,
故答案为:①温度计水银球应处于蒸馏烧瓶支管口处;②冷却水的方向通反了;
Ⅱ.乙烯和溴发生加成反应生成1,2-二溴乙烷,化学方程式为CH2═CH2+Br2→CH2BrCH2Br,
故答案为:CH2═CH2+Br2→CH2BrCH2Br.
你哪条
中文名称: 氯乙烷 英文名称: chloroethane 中文名称2:乙基氯 英文名称2:ethyl chloride CAS No.: 75-00-3 分子式: C2H5Cl 分子量: 64.52 理化特性 主要成分: 纯品 外观与性状: 无色气体,有类似醚样的气味。 熔点(℃): -140.8 沸点(℃): 12.5 相对密度(水=1): 0.92 相对蒸气密度(空气=1): 2.20 饱和蒸气压(kPa): 53.32(-3.9℃) 燃烧热(kJ/mol): 1349.3 临界温度(℃): 187.2 临界压力(MPa): 5.23 辛醇/水分配系数的对数值: 1.54 闪点(℃): -43(O.C) 引燃温度(℃): 510 爆炸上限%(V/V): 14.8 爆炸下限%(V/V): 3.6 溶解性: 微溶于水,可混溶于多数有机溶剂。
主要用途
要用作四乙基铅、乙基纤维素及乙基咔唑染料等的原料。也用作烟雾剂、冷冻剂、局部剂、杀虫剂、乙基化剂、烯烃聚合溶剂、汽油抗震剂等。还用作聚丙烯的催化剂,磷、硫、油脂、树脂、蜡等的溶剂。农药、染料、医药及其中间体的合成。
健康危害
有刺激和作用。高浓度损害心、肝、肾。吸入2%~4%浓度时可引起运动失调、轻度痛觉减退,并很快出现知觉消失,但其刺激作用非常轻微;高浓度接触引起,出现中枢抑制,可出现循环和呼吸抑制。皮肤接触后可因局部迅速降温,造成冻伤。 燃爆危险: 本品易燃,具刺激性。
氯乙烯又名乙烯基氯(Vinyl chloride)是一种应用于高分子化工的重要的单体,可由乙烯或乙炔制得。为无色、易液化气体,沸点-13.9℃,临界温度142℃,临界压力5.22MPa。氯乙烯是有毒物质,肝癌与长期吸入和接触氯乙烯有关。它与空气形成爆炸混合物,爆炸极限4%~22%(体积),在压力下更易爆炸,贮运时必须注意容器的密闭及氮封,并应添加少量阻聚剂。
CAS No.: 75-01-4 分子式: C2H3Cl 结构式: CHCl=CH2 分子量: 62.50 有害物成分 含量 CAS No. 氯乙烯 ≥99.99% 75-01-4 主要成分: 含量: 纯度≥99.99%。 外观与性状: 无色、有醚样气味的气体。 pH:无意义 熔点(℃): -159.8 沸点(℃): -13.4 相对密度(水=1): 0.91 相对蒸气密度(空气=1): 2.15 饱和蒸气压(kPa): 346.53(25℃) 燃烧热(kJ/mol): 无资料 临界温度(℃): 142 临界压力(MPa): 5.60 辛醇/水分配系数的对数值: 1.38 闪点(℃): 无意义 引燃温度(℃): 415 爆炸上限%(V/V): 31.0 爆炸下限%(V/V): 3.6
聚氯乙烯的结构式为[CH2-CHCl]n,是由氯乙烯单体通过自由基聚合而成的一种聚合物,英文名polyvinyl chloride,缩写为PVC。聚氯乙稀树脂为白色或浅**粉末,透明度胜于聚乙烯、聚丙烯,差于聚苯乙烯。它是世界上使用量最大的树脂之一,价格便宜,应用广泛, 其制品形式十分丰富,可分为硬聚氯乙烯、软聚氯乙烯、聚氯乙烯糊三大类。硬聚氯乙烯的硬度高于低密度聚乙烯,而低于聚丙烯,在屈折处会出现白化现象。主要用于管材、门窗型材、片材等挤出产品,以及管接头、电气零件等注塑件和挤出吹型的瓶类产品,它们约占聚氯乙烯65%以上的消耗。软聚氯乙烯主要用于压延片、汽车内饰品、手袋、薄膜、标签、电线电缆、医用制品等。聚氯乙烯糊约占聚氯乙烯制品的10%,主要用产品有搪塑制品等。
PVC粉状树脂可以按照粉状树脂的结构不同分为紧密型和疏松型两种:紧密型呈乒乓球状,吸收增塑剂的能力低,主要用于硬质PVC制品的生产;疏松型呈棉花团状,可大量吸收增塑剂,常用于软质PVC的生产。
聚氯乙稀有较好的电气绝缘性能,可作低频绝缘材料,其化学稳定性也好。由于聚氯乙稀的热稳定性较差,长时间加热会导致分解,放出HCL气体,使聚氯乙稀变色,所以其应用范围较窄,使用温度一般在-15~55度之间。
PVC按分子量的大小可分为通用型和高聚合度型两大类。通用型PVC的平均聚合度为500~1800,高聚合度型PVC的平均聚合度则大于1800。常用的PVC树脂大多为通用型。
1.PVC一般软制品。
利用挤出机可以挤成软管、电缆、电线等;利用注射成型机配合各种模具,可制成塑料凉鞋、鞋底、拖鞋、玩具、汽车配件等。
2.PVC薄膜。
PVC与添加剂混合、塑化后,利用三辊或四辊压延机可制成规定厚度的透明或有色薄膜。这些压延成型的薄膜可以通过剪裁,热合加工包装袋、雨衣、桌布、窗帘、广告膜、充气玩具等。宽幅的透明薄膜可以供温室、塑料大棚及地膜之用。经双向拉伸的薄膜,所受热收缩的特性,可用于收缩包装。同时。PVC薄膜是最好的三维表面膜制作材料。
3.PVC人造革。
有衬底的人造革是将PVC糊涂敷于布上或纸上,然后在100摄氏度以上塑化而成。也可以先将PVC与助剂压延成薄膜,再与衬底压合而成。无衬底的人造革则是直接由压延机压延成一定厚度的软制薄片,再压上花纹即可。人造革可以用来制作皮箱、皮包、书的封面、沙发及汽车的坐垫等,还有地板革,用作建筑物的铺地材料。
4.PVC泡沫制品。
软质PVC混炼时,加入适量的发泡剂做成片材,经发泡成型为泡沫塑料,可作泡沫拖鞋、凉鞋、鞋垫、及防震缓冲包装材料。也可用挤出机基础成低发泡PVC板材和异型材,可替代木材试用,是一种新型的建筑才材料。
5.PVC透明片材。
PVC中加冲击改性剂和有机锡稳定剂,经混合、塑化、压延而成为透明的片材。利用热成型可以做成薄壁透明容器或用于真空吸塑包装,是优良的包装材料和装饰材料。
6.PVC硬板和板材。
PVC中加入稳定剂、润滑剂和填料,经混炼后,用挤出机可挤出各种口径的硬管、异型管、波纹管,用作下水管、饮水管、电线套管或楼梯扶手。将压延好的薄片重叠热压,可制成各种厚度的硬质板材。板材可以切割成所需的形状,然后利用PVC焊条用热空气焊接成各种耐化学腐蚀的贮槽、风道及容器等。
7.PVC其它用途。
门窗有硬质异型材料组装而成。在有些国家已与木门窗铝窗等共同占据门窗的市场;仿木材料、代钢建材(北方、海边);中空容器;一次性医疗器械产品
甲烷分子中两个氢原子被氯取代而生成的化合物,分子式CH2Cl2。二氯甲烷是无色、透明、比水重、易挥发的液体,有类似醚的气味和甜味,不燃烧,但与高浓度氧混合后形成爆炸的混合物。二氯甲烷微溶于水,与绝大多数常用的有机溶剂互溶,与其他含氯溶剂、、乙醇也可以任意比例混溶。室温下二氯甲烷难溶于液氨中,能很快溶解在酚、醛、酮、冰醋酸、磷酸三乙酯、甲酰胺、环己胺、乙酰乙酸乙酯中。纯二氯甲烷无闪点,含等体积的二氯甲烷和汽油、溶剂石脑油或甲苯的溶剂混合物是不易燃的,然而当二氯甲烷与丙酮或甲醇液体以 10 :1 比例混合时,其混合特具有闪点,蒸气与空气形成爆炸性混合物,爆炸极限6.2%~15.0%(体积)。二氯甲烷是甲烷氯化物中毒性最小的,其毒性仅为四氯化碳毒性的 0.11% 。如果二氯甲烷直接溅入眼中,有疼痛感并有腐蚀作用。二氯甲烷的蒸汽有作用。当发生严惩的中毒危险时应立即脱离接触并移至新鲜空气处,一些中毒症状就会得到缓解或消失,不会引起持久性的损害。
二氯甲烷-物化性质
外观与性状:无色透明易挥发液体。具有类似醚的刺激性气味 沸点:39.8℃ 蒸汽压:30.55kPa(10℃) 熔 点:-95.1℃ 相对密度:1.3266(20/4℃) 水溶性:20 G/L (20 ?C) 自燃点:640℃。 粘度(20℃):0.43mPa?s。 折射率nD(20℃):1.4244。 临界温度:237℃, 临界压力:6.0795MPa。
溶解性:溶于约50倍的水,溶于酚、醛、酮、冰醋酸、磷酸三乙酯、乙酰乙酸乙酯、环己胺。与其他氯代烃溶剂乙醇、和N,N-二甲基甲酰胺混溶。
热解后产生HCl和痕量的光气,与水长期加热,生成甲醛和HCl。进一步氯化,可得CHCl3和CCl4。无色易挥发液体。难燃烧。蒸气与空气形成爆炸性混合物,爆炸极限6.2%~15.0%(体积)。二氯甲烷与氢氧化钠作用生成甲醛。工业中,二氯甲烷由天然气与氯气反应制得,经过精馏得到纯品,是优良的有机溶剂,常用来代替易燃的石油醚、等,并可用作牙科局部剂、制冷剂和灭火剂等。对皮肤和粘膜的刺激性比氯仿稍强,使用高浓度二氯甲烷时应注意。
安定性:在一般温度(常温)下没有湿气时,二氯甲烷比其同类物质(氯仿及四氯化碳)稳定。
危害分解性:长期与水接触会缓慢分解产生氯化氢。
危害之聚合:不会发生。
反应性及不相容性:
1.一般金属:於室温下使其少许的分解。
2.当受相当於或少於 25 克**的震荡时,二氯甲烷与四氧化二氮的混合物具有爆炸性。
3.与锂的碎片混合,对震荡很敏感且会爆炸,有时爆炸程度相当剧烈。
4.如果空气中含有高浓度的氧气,或在液态氧中,以及在四氧化氮中有钾、钠、钾-钠合金,种种状况下都会形成爆炸性混合物。
5.硝酸:形成爆炸性产物。
6.强氧化剂:可能起爆炸性反应。
7.强酸:可能起爆炸性反应。
8.铁、某些不锈钢、铜及镍:高温及水存在下会腐蚀此类金属。
9.铝粉:於适当压力,95℃下会产生无法控制的放热反应。
10.胺类:放热反应。
11.会与下列化合物激烈反应:胺类、锂、硝酸、钾化钠、、、、、
12.塑胶、橡皮、和一些涂料表层会被分解。
13.有可能聚集静电荷而引发蒸汽爆炸。
二氯甲烷-用途
二氯甲烷具有溶解能力强和毒性低的优点,大量用于制造安全**胶片、聚碳酸酯,其余用作涂料溶剂、金属脱脂剂,气烟雾喷射剂、聚氨酯发泡剂、脱模剂、脱漆剂。
二氯甲烷为无色液体,在制药工业中做反应介质,用于制备氨苄青霉素、羟苄青霉素和先锋霉素等;还用作胶片生产中的溶剂、石油脱蜡溶剂、气溶胶推进剂、有机合成萃取剂、聚氨酯等泡沫塑料生产用发泡剂和金属清洗剂等。
二氯甲烷在中国主要用于胶片生产和医药领域。其中用于胶片生产的消费量占总消费量的50%,医药方面占总消费量的20%,清洗剂及化工行业消费量占总消费量的20%,其他方面占10%。
二氯甲烷-危害
环境影响
该物质对环境可能有危害,在地下水中有蓄积作用。对水生生物应给特别注意。还应注意对大气的污染。
健康危害
侵入途径:吸入、食入、经皮吸收。
健康危害:本品有作用,主要损害中枢神经和呼吸系统。人类接触的主要途径是吸入。已经测得,在室内的生产环境中,当使用二氯甲烷作除漆剂时,有高浓度的二氯甲烷存在。一般人群通过周围空气、饮用水和食品的接触,剂量要低得多。据估计,在二氯甲烷的世界产量中,大约80%被释放到大气中去,但是由于该化合物光解的速率很快,使之不可能在大气中蓄积。其初始降解产物为光气和一氧化碳,进而再转变成二氧化碳和盐酸。当二氯甲烷存在于地表水中时,其大部分将蒸发。有氧存在时,则易于生物降解,因而生物蓄积似乎不大可能。但对其在土壤中的行为尚须测定。
健康危害效应:
急性:1.鼻子及喉咙的轻微刺激。
2.於500~1,000 ppm 1~2小时可能会导致中枢神经系统的轻度抑制,如:头晕、头昏眼花、恶心、手脚麻木、疲劳,无法集中精神及协调性减低。
3.非常高浓度暴露可能导致丧失意识及死亡。
皮肤:1.液体会刺激皮肤。
2.如流入手套内、鞋内或紧的衣内可能会严重刺激。
眼睛:1.液体及高浓度蒸气可能造成刺激。
2.液体可能导致角膜的短暂刺激。
食入:1.於动物实验中,二氯甲烷会被迅速吸收入体内造成中度毒性,症状如吸入。
慢性:1.吸入:於非常高浓度会造成肝及肾的损伤。亦有报告指出一再暴露於500~3,600 ppm会造成脑损伤。
2.致癌性:三研究指出长期暴露的工人并无癌症增多的迹象,但IARC将其列为疑似致癌物
氟利昂几种氟氯代甲烷和氟氯代乙烷的总称,主要是含氟和氯的烷烃衍生物,少数是环烷烃卤素衍生物,有的还含有溴原子。包括CCl3F(F-11)、CCl2F2(F-12)、CClF3(F-13)、CHCl2F(F-21)、CHClF2(F-22)、FCl2C-CClF2(F-113)、F2ClC-CClF2(F-114)、C2H4F2(F-152)、C2ClF5(F-115)、C2H3F3(F143)等等。以上氟里昂在常温下都是无色气体或易挥发液体,略有香味,低毒,化学性质稳定。其中最重要的是二氯二氟甲烷CCl2F2(F-12)。二氯二氟甲烷在常温常压下为无色气体;熔点-158℃,沸点-29.8℃,密度1.486克/厘米(-30℃);稍溶于水,易溶于乙醇、;与酸、碱不反应。二氯二氟甲烷可由四氯化碳与无水氟化氢在催化剂存在下反应制得,反应产物主要是二氯二氟甲烷,还有CCl3F和CClF3,可通过分馏将CCl2F2分离出来。
氟利昂-用途
由于氟利昂化学性质稳定,具有不燃、无毒、介电常数低、临界温度高、易液化等特性,因而广泛用作冷冻设备和空气调节装置的制冷剂。
氟利昂制冷剂
氟里昂制冷剂大致分为3类。
一是氯氟烃类产品,简称CFC。主要包括R11、R12、R113、R114、R115、R500、R502等,由于对臭氧层的破坏作用以及最大,被《蒙特利尔议定书》列为一类受控物质。
二是氢氯氟烃类产品,简称HCFC。主要包括R22、R123、R141b、R142b等,臭氧层破坏系数仅仅是R11的百分之几,因此,目前HCFC类物质被视为CFC类物质的最重要的过渡性替代物质。在《蒙特利尔议定书》中R22被限定2020年淘汰,R123被限定2030年。
三是氢氟烃类:简称HFC。主要包括R134A、R125、R32、R407C、R410A、R152等,臭氧层破坏系数为0,但是气候变暖潜能值很高。在《蒙特利尔议定书》没有规定其使用期限,在《联合国气候变化框架公约》京都议定书中定性为温室气体。
专家表示:我们目前所使用的所有制冷剂全部都是氟里昂制品,非氟里昂制冷剂到目前为止还没有研发出来。明令禁止的是第一类氯氟烃类产品,对于氢氯氟烃类产品和氢氟烃类制冷剂,还要有相当长的一段使用时间。所以,消费者千万不要谈“氟”色变。
此外,也大量用作雾化剂的组分,但由于它可能破坏大气臭氧层,现已限制使用。氟利昂的另一重要应用是作聚氨酯、聚苯乙烯和聚乙烯等泡沫塑料的发泡剂。R-113、R-11与其他溶剂的混合物还广泛用于电子工业和航空工业中作为溶剂,在纺织工业中用作纺织染整助剂(如整理油剂和洗涤剂)。氟利昂还是生产氟树脂的原料。由R-22可以生产四氟乙烯;由R-113可以生产三氟氯乙烯。三氟溴甲烷和1,1,2,2-四氟-1,2-二溴乙烷是效果良好的灭火剂,1,1,1-三氟-二氯-二溴乙烷可作为剂
氟利昂-危害
氟里昂是臭氧层破坏的元凶,它是本世纪20年代合成的,其化学性质稳定,不具有可燃性和毒性,被当作制冷剂、发泡剂和清洗剂,广泛用于家用电器、泡沫塑料、日用化学品、汽车、消防器材等领域。80年代后期,氟利昂的生产达到了高峰,产量达到了144万吨。在对氟利昂实行控制之前,全世界向大气中排放的氟利昂已达到了2000万吨。由于它们在大气中的平均寿命达数百年,所以排放的大部分仍留在大气层中,其中大部分仍然停留在对流层,一小部分升入平流层。在对流层相当稳定的氟利昂,在上升进入平流层后,在一定的气象条件下,会在强烈紫外线的作用下被分解,分解释放出的氯原子同臭氧会发生连锁反应,不断破坏臭氧分子。科学家估计一个氯原子可以破坏数万个臭氧分根据资料,2003年臭氧空洞面积已达2500万平方公里。臭氧层被大量损耗后,吸收紫外线辐射的能力大大减弱,导致到达地球表面的紫外线B明显增加,给人类健康和生态环境带来多方面的危害。据分析,平流层臭氧减少1%%,全球白内障的发病率将增加0.6-0.8%,即意味着因此引起失明的人数将增加1万到1.5万人。
由于氟里昂在大气中的平均寿命达数百年,所以排放的大部分仍滞留在大气层中,其中大部分停留在对流层,小部分升入平流层。
在对流层的氟里昂分子很稳定,几乎不发生化学反应。但是,当它们上升到平流层后,会在强烈紫外线的作用下被分解,含氯的氟里昂分子会离解出氯原子,然后同臭氧发生连锁反应(氯原子与臭氧分子反应,生成氧气分子和一氧化氯基;一氧化氯基不稳定,很快又变回氯原子,氯原子又与臭氧反应生成氧气和一氧化氯基……),不断破坏臭氧分子。
物质:四氟乙烯
化学品英文名称:tetrafluoroethylene
中文名称2:全氟乙烯
英文名称2:TFE 分子式:C2F4 分子量:100.01 CAS号:116-14-3
性质:无色无臭气体。熔点-142.5℃,沸点-76.3℃,不溶于水。比空气重。相对密度1.519,临界温度33.3℃,临界压力3.92MPa,燃点620℃。溶于丙酮、乙醇。自燃极限为11%-60%(体积),引燃温度只有180℃。有氧存在时,易形成不稳定易爆炸的过氧化物。 制备方法:二氟一氯甲烷经气化、预热、通入裂解炉,热裂解产含四氟乙烯单体的裂化气,经水洗、碱洗、压缩、冷冻脱水、干燥,分馏等工序,最后精馏得成品。
用途:制造聚四氟乙烯及其他氟塑料、氟橡胶和全氟丙烯的单体。可用作制造新型的热塑料、工程塑料、耐油耐低温橡胶、新型灭火剂和抑雾剂的原料。
健康危害:急性中毒:轻者有咳嗽、胸闷、头晕、乏力、恶心等;较重者出现化学性肺炎或间质型肺水肿;严重者出现肺水肿及心肌损害。吸入有机氟聚合物热解物后,可引起氟聚合物烟尘热。慢性中毒:常见有头痛、头晕、乏力、睡眠障碍等神经衰弱综合征和(或)腰背酸痛症状。可致骨骼损害。 环境危害:对大气可造成污染。 燃爆危险:本品易燃。
主要成分: 纯品 外观与性状: 无色液体,有氯仿样气味。 熔点(℃): -22.2 (有报道-22.35;-22.7) 沸点(℃): 121.2 相对密度(水=1):(20℃/4℃)1.6226 相对蒸气密度(空气=1): 5.83 饱和蒸气压(kPa): 2.11(20℃) 燃烧热(kJ/mol): 679.3 临界温度(℃): 347.1 临界压力(MPa): 9.74 折射率1.50566 辛醇/水分配系数的对数值: 2.88 溶解性: 不溶于水(溶于约10000倍体积的水),可混溶于乙醇、等多数有机溶剂。
主要用途
用作溶剂。
危险品信息
健康危害本品有刺激和作用。吸入急性中毒者有上呼吸道刺激症状、流泪、流涎。随之出现头晕、头痛、恶心、运动失调及酒醉样症状。口服后出现头晕、头痛、倦睡、恶心、呕吐、腹痛、视力模糊、四肢麻木,甚至出现兴奋不安、抽搐乃至昏迷,可致死。慢性影响:有乏力、眩晕、恶心、酩酊感等。可有肝损害。皮肤反复接触,可致皮炎和。
燃爆危害本品可燃,有毒,具刺激性。
七氟丙烷
性质:无色的无气味气体,微溶于水
用途:灭火剂的原料,发射火箭的湿剂,配药测量的药量吸入器
危害:
四氯化碳为无色澄清易流动的液体,工业上有时因含杂质呈微**,具有芳香气味,易挥发。密度(20℃)1.595克/立方厘米、熔点-22.8℃,沸点76~77℃。 四氯化碳的蒸气较空气重约5倍,且不会燃烧。四氯化碳的蒸气有毒,它的性较氯仿为低,但毒性较高。吸入人体2~4毫升就可使人死亡。 四氯化碳在水中的溶解度很小,且遇湿气及光即逐渐分解生成盐酸。易溶于各种有机溶剂,能与醇、醚、氯仿、苯等任意混合。对于脂肪、油类及多种有机化合物为一极优良的溶剂。
四氯化碳用作灭火剂时,不能灭活泼金属的火,因为活泼金属可以与之反应
DDT又叫滴滴涕,二二三,化学名为双对氯苯基三氯乙烷(Dichlorodiphenyltrichloroethane),化学式(ClC6H4)2CH(CCl3)。中文名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂。为20世纪上半叶防止农业病虫害,减轻疟疾伤寒等蚊蝇传播的疾病危害起到了不小的作用。
轻度中毒可出现头痛、头晕、无力、出汗、失眠、恶心、呕吐,偶有手及手指肌肉抽动震颤等症状。重度中毒常伴发高烧、多汗、呕吐、腹泻;神经系统兴奋,上、下肢和面部肌肉呈强直性抽搐,并有癫痫样抽搐、惊厥发作;出现呼吸障碍、呼吸困难、紫绀、有时有肺水肿,甚至呼吸衰竭;对肝肾脏器损害,使肝肿大,肝功能改变;少尿、无尿、尿中有蛋白、红细胞等;对皮肤刺激可发生红肿、灼烧感、瘙痒,还可有皮炎发生,如溅入眼内,可使眼暂性失明。DDT一般毒性与六六六相同,属神经及实质脏器毒物,对人和大多数其它生物体具有中等强度的急性毒性。它能经皮肤吸收,是接触中毒的典型代表,由于其在常压时即使在12℃以下,也有一定的蒸发,所以吸入DDT蒸气亦能引起中毒。对人不论是故意的或是过失造成大量服用时,即能引起中毒
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。